Diabetes en medicatie Kennisonderwerp
Verschillende vormen, risicostratificatie en antidiabetica
Basiskennis diabetes
- Ca 5% DM2 is eigenlijk MODY en 15% LADA.
- Vooral bij BMI < 27 kg/m2 of indien patiënt niet goed reageert op orale medicatie: denk aan MODY of LADA
- Roken verlaagt de insulinegevoeligheid. Stoppen met roken verhoogt dit.
- In eerste decennium 2000 ondanks verbeterende landelijke behandeling DM, geen reductie sterfte door HVZ. Wél na introductie SGLT2-remmers en GLP1-receptoragonisten. SGLT2 doet het net iets beter en kost minder, mogelijk over 5 jaar standaard add-on naast metformine. Niet zozeer voor verlaging glucose, als wel als cardioprotectie.[1]
- Pre-diatetes (impaired glucose tolerance or impaired fasting glucose): combinatie metformine en leefstijlinterventie verlaagt risico op ontwikkelen diabetes met 17% tov alleen leefstijl (HR 0.83, ARR 19.8% -> 17.3%)[2]
- Iedereen met diabetes en hartinfarct een SGLT2
Diagnose
- 2x nuchter glucose ≥ 7,0 mmol/L op 2 verschillende dagen
- icm klachten passend bij hyperglykemie:
- nuchter glucose ≥ 7,0 mmol/L of willekeurige glucose ≥ 11,1 mmol/L
- Serumglucose! Vingerprik draagbare POC glucosemeter: afwijking 10-15%, dus vanuit het lab
- 6,2-7,0: "gestoorde glucosewaarde"
- Stoppen met roken en 5 kg afvallen groot gunstig effect
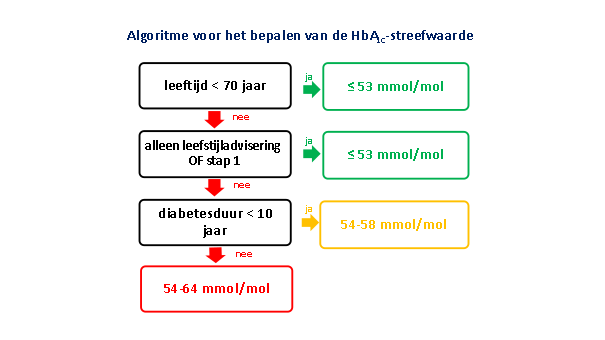
- Normaalwaarde/streefwaarden HbA1c per leeftijd[3]
NHG[4] - HbA1c kan verhoogd zijn bij H. Pylori zonder DM
- Kan vals normaal zijn bij hemolyse → fructosamine bepalen
- Niet-diabeten
- 20-42 mmol/mol
- ≥48 = diabetes in internationale literatuur
- Diabeten <70 jaar
- ≤53
- Diabeten ≥70 jaar
- Alleen dieet of metformine monotherapie: ≤53
- Ziekteduur korter dan 10 jaar vanaf behandelstap 2: 54-58
- Ziekteduur van 10 jaar of langer vanaf behandelstap 2: 54-64
- Levensverwachting < 5 jaar: 53-69; behandeling gericht op voorkomen hypo- of hyperglycemische ontregeling
- Curve
- 4-puntscurve
- Nuchter ochtend, voor de lunch, voor avondeten en voor slapen
- 7-puntscurve link
- Nuchter ochtend en 1.5 uur na ontbijt, voor en 1.5 uur na de lunch, voor en 1.5 uur na avondeten en voor slapen
- 4-puntscurve
Bepaal bij iedere patiënt
- Heeft deze patiënt zeer hoog risico?
- Welk stappenplan volg ik?
- Wat bepaalt zijn zeer hoge risico? Ischemie? Hartfalen? Nierfalen?
- Wat is de streefwaarde voor HbA1c?
- Welke riscifacgtoren zijn aanwezig bij de patiënt zonder zeer hoog risico?
Risicofactoren inventariseren
Zeerhoogrisico[5]
- HVZ (met DM 2x hoger risico op opname en/of overlijden aan HVZ)
- Doorgemaakt ischemische HVZ (incl AP en TIA) of aortasclerose/aneurysma/PAV
- Hartfalen (onafhankelijk van ejectiefractie[6]) -> dan sowieso SGLT2
- CNS
- eGFR ≥ 60 ml/min/1,73 m2 met ACR > 30 mg/mmol
- eGFR 45-59 ml/min/1,73 m2 met ACR > 3 mg/mmol
- eGFR 10-44 ml/min/1,73 m2
- Indien niet-kwetsbaar, met levensverwachting >5 jaar: volg stappenplan
Verder
- Familienamnese
- vader, moeder, broer of zus met HVZ < 65 jaar
- Leefstijl
- roken, lichamelijke activiteit, voedingsgewoonten, alcoholgebruik.
- RR en BMI
- CVRM-lab
Behandeling
Altijd
- Voorlichting/educatie DM
- Niet-medicamenteuze adviezen: niet roken, voldoende lichaamsbeweging, afvallen bij BMI > 25, gezonde voeding; verwijs naar een diëtist.
Standaard
- Metformine
- Hoger dan 1000mg 2dd niet erg effectief
- Voeg een sulfonylureumderivaat toe (bij voorkeur gliclazide)
- Voeg (middel)langwerkende insuline eenmaal daags toe (bij voorkeur NPH-insuline)
- Alternatief: DPP4-remmer of GLP1-agonist (*bij BMI ≥ 30 of hoger en HbA1c < 15 mmol/mol boven de streefwaarde ivm onvoldoende hyperglycemische controle van GLP-1 tov insuline, zie tabel 11 NHG)
- Intensiveer insulinebehandeling
- Alternatief: DPP4-remmer of GLP1-agonist*
Zeer hoog risico
Behandeling heeft meer te maken met verlagen risico morbiditeit/mortaliteit door HVZ en nierfalen, dan met reguleren glucose.- SGLT2-remmer (ivm gunstig effect HVZ). Bij contra-indicatie voor SGLT2-remmer (bijvoorbeeld eGFR < 30 ml/min/1,73 m2 , zie ook tabel 9): start GLP1-receptoragonist*
- Dapagliflozide 10mg (gunstiger kosten dan empagliflozine, zelfde conditie nierfunctie; empagliflozine is zowel 10 als 25 mg beschikbaar
- Voeg metformine toe
- Voeg een GLP1-receptoragonist toe bij een HbA1c < 15 mmol/mol boven de streefwaarde, zie tabel 11 NHG*
- evt ophogen bij enig effect
- bij geen effect, overweeg insuline (+GLP-1-ra en metformine)
- Voeg een van de middelen uit het stappenplan voor patiënten zonder zeer hoog risico toe (combinatie van GLP1-receptoragonist met DPP4-remmer is niet rationeel en wordt ontraden)
SGLT2-remmer geïndiceerd bij decompensatio cardis vanaf NYHA II, ook zonder diabetes. SGLT2-remmer verlaagt risico hyperkaliëmie bij DM+hoogrisico of CNS zonder kans hypokaliëmie.[7][8]
- Misvatting: een SGTL-2 remmer ivm hartfalen stelt DM2 uit. Namelijk bij personen met pre-diabetes leidt stoppen met DM-medicatie tot net zoveel diagnoses DM2 als bij placebo.[9]
Hypoglycemie
- Serumglucose < 3,5 mmol/L met de daarbij passende symptomen.
- Advies: 6 dextro's OF 16-20 gram suiker OF 2 eetlepels suiker opgelost in water. Daarna 2 boterhammen met zoet beleg.
- Evt na 15 min gluc meten en na 1 uur. Bij onvoldoende resultaat (gluc ≥ 5,0 mmol/L): herhaal schema. Indien dan geen verbetering: contact.
- Behandeling medisch: glucagon i.m. (effect na 15 min) glucose 50% 10ml
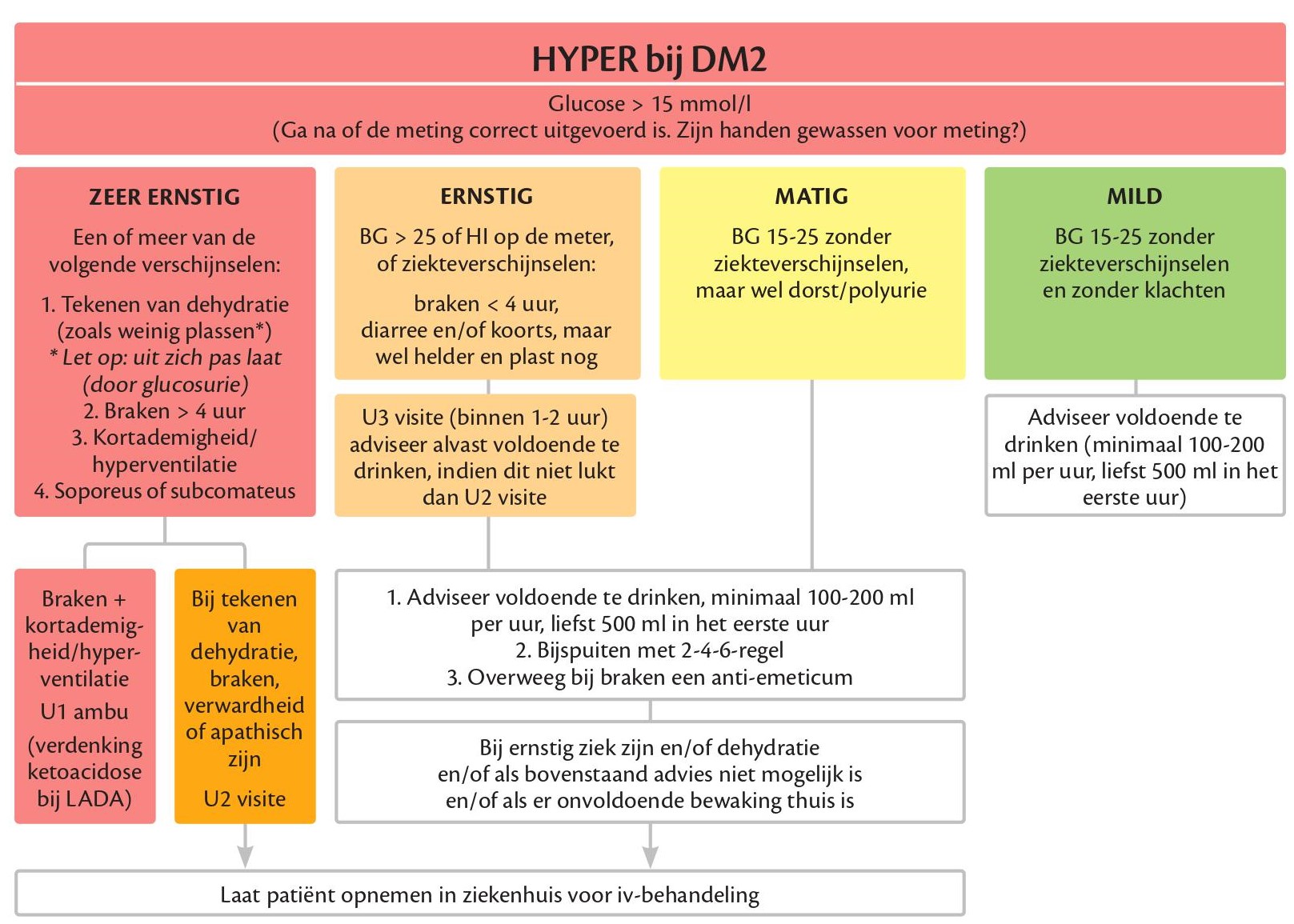
Hyperglycemie
- 2-4-6-regel voor serumglucose > 15 mmol/L
- Iedere twee uur meten tot bloedglucose < 15 mmol/l
- 4 E extra insuline toedienen bij bloedglucose 15-20 mmol/L
- 6 E extra insuline toedienen bij bloedglucose> 20 mmol/L
- Dit moet een snel-/kortwerkend insuline zijn
- Ga hiermee door tot bloedglucose < 15 mmol/L
- Toediening extra vocht
- Regel van 100: hoeveel daalt serumglucose op 1 E kortwerkende insuline
- 100/TDD (totale dagdosering insuline)
- Bijv TDD (= basaal + bolus) = 50 E
- 100/50 E = 2
- Bloedglucose daalt met 2,0 mmol/I op 1 E insuline
- 100/TDD (totale dagdosering insuline)
- Bij braken en DM2: denk aan HHS
Medicatie
SGLT2-remmers (Glifozines, natrium-glucose-cotransporter 2-remmers)
- Dapagliflozine (Forxiga, goedkoper) 1dd 10mg of Empagliflozine (Jardiance, €2.50 ipv €1.50/dag) 1dd 10mg. Bij GFR >30. Oraal.
- Beide beschikbaar als combinatietablet met metformine (5/850 of 5/1000 2x per dag)
- DM, hartfalen (ook los van DM), nierinsufficientie (ook los van DM)
- Blokkeert selectief en reversibel de SGLT2 in niertubuli. Hierdoor excretie natrium en glucose, leidt tevens tot osmotische diurese
- Dus glucosurie, daardoor meer UWI's, candida, balanitis
- Verlaging bloedglucose; daling bloeddruk (2-4mmHg), gewichtsverlies (2-4kg), lagere pre- en afterload -> verbetering LVF, vertraging progressie CNS.
- Tijdelijk staken bij symptomen normoglykemische (=euglykemische) ketoacidose
- Braken en hyperventileren → onderzoeken
- Incidentie 0 (0-2 meer) per 1000 na 5 jaar
- Ziekte = stress, leidt tot toegenomen insulinebehoefte
- Diabetische KA: relatief/absoluut tekort insuline waardoor onvermogen metabolisering glucose. Hierdoor ketonenmetabolisme, hyperglycaemie, osmotische diurese, glucosurie, hyperosmalaliteit, dehydratie en uiteindelijk ketoacidose.
- Bij SGLT-2 geen hyperglycemie door glucosurie
- Symptomen
- verminderde voedselinname
- koortsende ziekte
- misselijkheid en braken
- extreme dorst
- diarree
- voorafgaand aan chirurgische ingreep (ontregeling metanbole status; bij nuchter blijven?)
- = zelfde als bij metformine
- Contraindicaties: eGFR <30 bij start, recidiverende schimmelinfecties, ondervoeding/intermitterend vasten, alcoholisme, actief voetulcus
- niet-genezende wond aan de voet/gangreen van Fournier
- Betere nieruitkomsten. Vermindering morbiditeit/mortaliteit HVZ. Tevens indicatie bij decompensatio cordis zonder DM. Voor beide werkingsmechanisme nog niet duidelijk. Tevens nierfalen.
- Glifozins, a new class of diuretics that act by a new mechanism (lowering BP as well), have glucosuria as a relevant adverse effect in some patients, which is a limitation compared with traditional diuretics. The beneficial effect over uric acid, if sustained, is an advantage over thiazide diuretics, and may have clinical implications in managing patients prone to developing gout.[10]
GLP-1-agonisten (glucagon-like-peptide-1)
- Dulaglutide (Trulicity, 1x/week), liraglutide (Victoza, 1x/dag), semaglutide (Ozempic 1x/week). Subcutane injectie, semaglutide ook oraal.
- subcutaan: semaglutide 1x/wk 0,25 mg (max. 1x/wk 1 mg), liraglutide 1 dd 0,6 mg (max. 1 dd 1,8 mg), dulaglutide 1x/wk 1,5 mg (max. 1x/wk 4,5 mg)
- oraal: semaglutide (Rybelsus) begindosis 3 mg 1×/dag; na 1 maand moet de dosering worden verhoogd naar 7 mg 1×/dag. Na ten minste 1 maand met een dosering van 7 mg 1×/dag, de dosering zo nodig verder verhogen naar max. 14 mg 1×/dag.
- Effectiviteit op cardiovasculaire eindpunten betwist, onderzoek gaande. Ander bezwaar tegen semaglutide oraal is dat het effect niet makkelijk te voorspellen is door:
- hoge variatie in absorptie tussen personen, en binnen persoon: de absorptie wordt minder bij gelijktijdige inname met voedsel of grote hoeveelheden water. Vasten na inname leidt juist weer tot een hogere absorptie.
- Effectiviteit op cardiovasculaire eindpunten betwist, onderzoek gaande. Ander bezwaar tegen semaglutide oraal is dat het effect niet makkelijk te voorspellen is door:
- Orfoglipron (oraal, small molecule, non-peptide)
- Activereert de GLP1-receptor, dit leidt tot: stimulering glucoseafhankelijke insulinesecretie door β-cellen van de pancreas; onderdrukking van de
- glucagonafgifte, waardoor de hepatische glucoseafgifte daalt; vertraging van de maaglediging, waardoor glucose uit voedsel minder snel wordt opgenomen; toename van verzadigingsgevoel en vermindering van het gevoel van trek en honger (liraglutide).
- Werkt ook beschermend op myocyten
- Bijwerkingen: misselijkheid (vol gevoel/verzadiging)
- Iets verhoogde kans schildklierkanker: HR 1.52-1.76. 5-year number needed to harm of 1349[13]
- Vermindering morbiditeit/mortaliteit HVZ alleen bij DM2. Werkt ook tegen obesias, maar dan levenslang innemen
- Vergoeding: formulier artsenverklaring invullen link, zie voorwaarden link
- Flowchart: link
- DM, BMI >35, onvoldoende regulatie glucose met metformine en gliclazide/SGLT2 in hoogste dosering
- Offlabel bij obesitas: zie Obesitas
DPP-4 inhibitors (gliptines)
- Sitagliptine (Januvia). Oraal.
- 100 mg 1×/dag bij GFR > 45
- Zorgt ervoor dat lichaamseigen GLP-1 langer in het lichaam blijft (inactivatie van GLP-1 vertraagd). Nooit samen met GLP-1.
- Voorkomt hydrolyse van incretinehormonen door DPP-4. Hierdoor stijgen plasmaconcentraties van actief GLP-1 en GIP (glucose-afhankelijke insulinotrope polypeptide). Dit leidt tot: stimulering glucoseafhankelijke insulinesecretie door β-cellen en onderdrukking glucagonafgifte waardoor verlaging bloedglucose.
- Bijwerking: vaker cholecystitis (OR 1.43) en galblaasaandoeningen in het algemeen (OR 1.22)[14]
Insuline (bijna alle pennen bevatten 300 EH in 3 ml)
- Alle patiënten met DM2 en insuline: braken = bellen (ivm risico HHS)
- "Langwerkend" insuline bestaat eigenlijk niet, alleen vertraagde resorberende
- Kort (max na 45-90 min, uitwerking na 4-5 uur)
- Novorapid / aspart
- Humalog / lispro
- Apidra / glulisine
- (Middel)langwerkende humane NPH-insuline (max na 4-6 uur, uitwerking na 16 uur). Te gebruiken bij DM2 gezien insulinebehoeftig en niet 24 uurs -afhankelijk. Werkt uitstekend op nachtelijke hyperglycemie te voorkomen. Weinig kans op hypo's (itt ultrastrak ingestelde onderzoekspopulatie).
- Humuline NPH
- Insulatard
- Steeds slechter beschikbaar[15]
- Insuman basal
- Langwerkende insuline-analoog (max na 4 uur, vlakke curve voor rest van etmaal)
- Glargine (Lantus, Abasaglar, Toujeo (hoger geconcentreerd. Niet superieur, met name marketing bij hogere prijs)) - dankzij injectie in zure oplossing
- Detemir (Levemir; iets trager en korter werkend)
- Ultralang werkend
- Degludec (Tresiba): max na 1 uur, vlak gedurende 24 uur. Peperduur
- Analoge mix-insuline (novomix, steeds minder in gebruik)
- combinatie van snelwerkende en NPH
- Voordeel: 2 keer per dag spuiten. Nadeel: weinig natuurlijk insuline/gluocosebeloop. Kan wel bij bejaarde patiënten met zeer regelmatig leven.
- 15 mmol/L belangrijke acute grens: toegenomen glucosurie, afname leukocytenfunctie
- 10,0 mmol/L grens voor glucosurie (renal threshold)[16]
- 10,5 mmol/L of HbA1c 64 mmol/mol bij chronische DM
- 10,0 mmol/L grens voor glucosurie (renal threshold)[16]
- Bij DM1 uitgebreid gunstige ervaring met insulinepomp. Dit blijkt voor DM2 ook betere glucoseregulatie te geven dan met handmatig spuiten.[17]
- Tijd in targetgebied met 14% toegenomen, andere uitkomsten ook beter, geen toegenomen kans hypo's
2-4-6-regel
- Kan alleen met snelwerkend insuline, alleen bij klinisch goed genoeg om thuis te blijven
- 2: iedere 2 uur BG meter, tot BG < 15 mmol/L
- 4 EH bij gluc 15-20 mmol/L
- 6 EH bij gluc > 20 mmol/L
Overige middelen (niet aangeraden in NHG standaard)[18]
Acarbose
De toepassing van acarbose wordt beperkt door het frequent optreden van darmklachten, met name flatulentie (minder bij langzaam optitreren). Op grond van vooral de langetermijnveiligheid is er een voorkeur voor acarbose boven pioglitazon.Pioglitazon
Pioglitazon gaat mogelijk gepaard met een verhoogd risico op fracturen en er is onduidelijkheid over het optreden van ernstige bijwerkingen, zoals blaaskanker, hartfalen en pneumonie.Repaglinide
Repaglinide is qua werkingsmechanisme te vergelijken met de SU-derivaten. Een voordeel van repaglinide is dat het vlak voor de maaltijd wordt ingenomen en de maaltijden niet op vaste tijdstippen hoeven plaats te vinden.
LADA (Latent Autoimmune Diabetes of the Adult)
- In feite gewoon DM1, meestal voor 40-60e levensjaar. Insuline optimale behandeling.
- 40-55 jaar met tekenen van hyperglycemie (dorst, veel plassen, gewichtsverlies)
- Vaak BMI < 28
- Verhoogd risico andere auto-immuunziekten, zoals schilkdlierfunctieafwijkingen en coeliakie
- 40-55 jaar met tekenen van hyperglycemie (dorst, veel plassen, gewichtsverlies)
- Diagnose dmv diabetesspecifieke autoantistoffen (meestal glutamaatdecarboxylase-antistoffen, anti-GAD)[19]
- Als anti-GAD negatief → behandelen als normale DM2
- Zegt niets over noodzaak insulinebehandeling; soms direct, soms pas na 3 jaar
- Doel insuline: voorkomen ketoacidose
- Vaak uitslag na een week, geen bijdrage aan eerste beoordeling
- Aanwezigheid autoantistoffen bevestigt diagnose. Afwezigheid sluit niet uit – kunnen na verloop van tijd negatief worden
- Bij aanhoudende twijfel kan in overleg met de kaderhuisarts diabetes deze bepaling eventueel worden overwogen.
- GAD65: positief vanaf 5 U/ml[20]
- Niet regulier aanbevolen:
- IA2: positief vanaf 8 U/ml
- ZnT8: positief vanaf 15 U/ml
- Niet regulier aanbevolen:
- Controleer urine op ketonen indien BG >15, indien positief/verdenking: verwijzing 2e lijn
- Orale behandeling is minder effectief dan bij type 2-diabetespatiënten. Start dan insuline.
- Géén SGLT2-remmer starten, relatieve contra-indicatie ivm risico keto-acidose
- Soms aanvankelijk per abuis als DM2 behandeld; al behandelend valt op dat streefwaarden lastig te halen zijn en orale antidiabetica onvoldoende effectief zijn. Stap op insuline, dan adequate behandeling
MODY (Maturity-onset diabetes of the young)
- Is geen probleem insulineresistentie, maar van betacel (niet-gehele insulinedeficientie). SU-derivaten goede behandeling.
- Positieve FA andere auto-immuunziekte
- Autosomaal dominant overervende aandoeningen waarbij een monogenetisch bètaceldefect
- Bij dragerschap: jaarlijks screening incl fructosamine
- Leeftijd <35, geen relatie gewicht en leefstijl
- Hyperglycemie vanaf de geboorte
- Metformine weinig effectief, gliclazide wel
- Afwezigheid keto-acidose
- Diagnose
- DNA-diagnostiek (in ziekenhuis)
- Vele verschillende subtypen link
- Verwijzing internist
Diabetes mellitus type 1
- Insuline afwezig → geen glucose in de cellen → lypolyse → productie ketonen → acidose
- Laat je niet misleiden op de HAP: 80-jarige patient met insuline mogelijk als DM2 ingeboekt, terwijl het type 1 betreft!
- Onderscheid door bepaling anti-GAD
- Urine stick
- Vals negatief: urinestick meet alleen AcAa, geen BHA (terwijl dat wél veel voor kan komen)
- acetoacetic acid (=3-oxobutaanzuur of acetoazijnzuur) vs β-hydroxybutyric acid (3-hydroxybutaanzuur)
- Vals positief: gebruik oa levodopa, valproaat; vitamine C, dehydratie, te weinig koolhydraten intake
- Vals negatief: urinestick meet alleen AcAa, geen BHA (terwijl dat wél veel voor kan komen)
Diabetes mellitus 2
- Hyperosmolair hyperglycemisch syndroom → glucosurie → patient droogt uit, mortaliteit 10-15%
- Leefstijl: niet alleen gewicht/afvallen maar zéker bewegen. Rollator maakt bereiken streefwaarde buitengewoon lastig
- In principe altijd nog (enige) insulinesecretie → géén ketoacidose (mits geen medicatie)
C-peptide[21]
Het C-peptide is een maat voor de eigen insulineproductie en bepaling daarvan in de tweede lijn kan soms nuttig zijn om onderscheid te maken tussen de verschillende typen diabetes. Deze bepaling laat zien of de bètacel zelf nog insuline maakt. Ze moet altijd gecombineerd worden met een nuchtere glucosebepaling, om een uitspraak over de eigen insulineproductie te kunnen doen. Het C-peptide moet immers hoger zijn bij een hogere glucosewaarde.Ook aan deze bepaling zitten haken en ogen ten tijde van de diagnose. Bij acute insulinedeficiëntie kunnen de C-peptidewaarden nog voldoende hoog lijken, terwijl behandeling van insuline al noodzakelijk is. Daarnaast duurt de uitslag van deze test een aantal dagen/weken en heeft de bepaling van het C-peptide dus geen meerwaarde tijdens de eerste beoordeling in de huisartsenpraktijk. Bij aanhoudende twijfel kan in overleg met de kaderhuisarts diabetes deze bepaling eventueel worden overwogen.
- C-peptide heb je random niets aan; vooral gebruikt om insulinoom te diagnosticeren. Eventueel in de vorm van HOMA als wetenschappelijk instrument, klinisch niet erg nuttig[22]
- Insuline + glucose = surrogaat voor insulineresistentiemeting (dus niet voor insulinedeficientie cq DM1 en LADA)
Acute diabetische ontregeling op de HAP (Langerhans)[23]
- Acute Diabetesgerelateerde problemen Langerhans link
- Hyper, hypo, verkeerde insuline gespoten, te veel EH of dubbel gespoten, vergeten te spuiten, wil niet eten maar moet spuiten
- Beslisboom hyperglykemie in de acute fase link
- Vraag: DM1 of DM2! Hoe lang al insuline? Welke medicatie? Leeftijd/BMI geen goede indicatie.
- Snelwerkende ipv langwerkende insuline gespoten voor de nacht
- Direct bloedglucosebepaling doen. Eerste 2-3 uur: minimaal iedere 30 minuten herhalen, tot ca 5 uur na injectie
- Insuline aspart: werking maximaal na 1–3 uur; werkingsduur: 3–5 uur.[24]
- Direct koolhydraten innemen. Hoeveelheid afhankelijk van aantal EH.
- Vraag naar aantal eenheden snelwerkende insuline dat normaal gespoten wordt voor maaltijd. Als nu 3x zoveel gespoten, een redelijk idee an hoeveel er nu gegeten moet worden.
- Boterham met jam/hagelslag, bord pasta (géén kaas)
- Langwerkenede insuline alsnog geven?
- DM1: halve dosis ochtend erna
- DM2: weglaten
- Direct bloedglucosebepaling doen. Eerste 2-3 uur: minimaal iedere 30 minuten herhalen, tot ca 5 uur na injectie
- Lang ipv snel
- Type 1 of type 2? Reden van vergissing, dd cognitieve achteruitgang?
- Direct BG
- Eerste 7 uur: ieder uur BG
- Vervolgens iedereen 1-2 uur tot max 24 uur
- Niet bijspuiten zolang normoglycemisch. Bij-eten ip niet nodig.
- Postnocturale forse hyperglycemie (bijv 19 mmol/L)
- veel te veel koolhydraten ingenomen
- normaal analoge mix 25 (32-0-18)
- beter niet behandelen met insuline, focus op voldoende vochtintake
- Bottom-line:
- niet iedere incidentele ontregeling behoeft insuline bijspuiten (wel bijspuiten is niet per se verkeerd, maar waarschijnlijk dan veel langere ontregeling vs weinig winst van bijspuiten bij incidentele hyperglycemie)
- misvatting dat bij braken en niet eten de insuline altijd moet worden verminderd (cave HHS)
- Dreigend Hyperosmolair hyperglykemisch syndroom, HHS
- Bij insuline-gebruikers
- Nog insulinesecretie aanwezig, lipolyse nog onderdrukte, geen sterke ketogenese
- Hyperglycemie veroorzaakt osmotische diurese, verhoogd risico dehydratie
- HHS heeft hoge mortaliteit (bij goede behandeling 10-15%)
- Uitlokkende factoren: o.a. infectie
- Bij insulinetherapie: braken = bellen
- Loopt vaak goed af, maar extra zorgvuldigheid vereist. Als aanhoudend braken, niet-zakkend glucose, mn glucose richting 30 etc. gluc rond 20 nog speling)
- Bij dreigende HHS, in goede toestand (braken <2-3 uur, compos mentis) met redelijk glucose dat reageert op insuline:
- Gewoon insuline spuiten volgens 2-4-6 (anders ketoacidose)
- Heel veel drinken (kleine hoeveelheden, 200ml/uur)
- Terug laten bellen met glucosewaarde na 2 uur, in eigen agenda zetten
- Bij ernstige HHS: plasma-glucose >30 → met spoed insturen
- Braken >3-4 uur
- Diabetische keto-acidose DKA
- Absoluut insulinetekort (cave soms ook bij DM2, mn bij mensen negroide en caribische achtergrond).
- Hyperglycemie, acidose, ketose
- Ernst hangst samen met mate van acidose
- Behandeling
- Absoluut insulinetekort (cave soms ook bij DM2, mn bij mensen negroide en caribische achtergrond).
Diabetetische controles
Voetenzorg en Sims-classificatie[26]
- Maak bij het testen van de protectieve sensibiliteit gebruik van een 10 grams Semmes-Weinstein monofilament, waarbij volstaan kan worden met het testen op drie eeltvrije plaatsen (plantaire zijde hallux, plantaire zijde metatarsale 1 en plantaire zijde metatarsale 5).
- Bepaal bij afwezige pulsaties (zowel van de a. dorsalis pedis als van de a. tibialis post.) een Doppler-signaalmeting en bij afwijkingen hiervan (mono- of bifasische tonen) een Enkel-Arm Index (EAI).
- Sims-classificatie vaststellen
- Vernoemd naar David S. Sims, die de combinatie van risicofactoren leidend door een voetulcus beschreef.
| Bevindingen | Classificatie | Frequentie voetonderzoek | Zorgprofiel | Vergoeding |
|---|---|---|---|---|
| Geen verlies PS of PAV (met of zonder zelfmanagement) | Sims 0 | - | 1 jaar | - |
| Verlies PS of PAV | Sims 1 | 1. Geen vergoeding voetbehandeling uit basisverzekering | 6 maanden | Praktijkondersteuner, diabetesverpleegkundige, (diabetes)podotherapeut, medisch pedicure |
| Verlies PS of PAV i.c.m. verhoogd risico op infectie of drukplekken | Sims 1 | 2. Vergoeding voetbehandeling uit basisverzekering | 3 maanden | |
| Verlies PS én PAV | Sims 2 | 3. Vergoeding voetbehandeling uit basisverzekering | 3 maanden | (Diabetes)podotherapeut, medisch pedicure voor signaleren en behandeling |
| Genezen ulcus, amputatie of inactieve Charcot | Sims 3 | 4. Vergoeding voetbehandeling uit basisverzekering | 1-3 maanden | (Diabetes)podotherapeut, eventueel multidisciplinair voetenteam |
| Actief ulcus | - | - | Ziekenhuiszorg | Multidisciplinair team |
Ramadan
Toolkits en posters Diabetes Federatie linkInsulinoom
Insulinoom geeft de trias van Whipple- lage bloedsuikers in nuchtere toestand
- neuroglykopenie (gedragsveranderingen, sufheid, insulten, coma) of evt transpireren, tremor, tachycardie.
- wat dan herstelt door suiker eten.
Casus HAP
- Exacerbatie COPD bij DM wv metformine en insuline detemir
- Prednison 30mg stootkuur
- Insulineresistentie cellen neemt toe, remt B-cel, stimuleert gluconeogenese
- Nuchtere waarde niet aangedaan, meet eind van de middag-avond → advies tussen 15-16 uur meten, dan contact EHA
- Wel behandelen als dreiging gluc >15
- Prednison 30mg stootkuur
- Hypoglycemie en bewustzijnsverlies
- Gebruikt patient SU-derivaat/langwerkende insuline die hypo mogelijk veroorzaakt heeft?
- Ja:
- Laat glucagon i.m/s.c. spuiten indien aanwezig
- glucagon nasaal (Baqsimi 3mg in 1 neusgat, eenmalig (cave niet in lucht spuiten: 1 dosis in spuit). Wordt passief opgenomen in slijmvlies)
- Spoedvisite U1
- Glucose i.v. minimaal 50-100 ml 10% (2e keus: 50% minimaal 20ml. Nadeel: erg lage pH → necrose indien IM of SC)
- Indien niet mogelijk om infuus te prikken: evt geconcentreerd buccaal toedienen
- Overweeg insturen bij lang aanhoudende hypo (bij langwerkende insuline)
- Laat glucagon i.m/s.c. spuiten indien aanwezig
- Nee:
- Laat glucagon i.m/s.c. spuiten indien aanwezig
- Spoedvisite U1
- Advies 2 boterhammen met zoet beleg
- Herhaal glucosewaarden 15 min, 1 uur en 2 uur → Laat waarden aan HAP doorbellen, noteren tijd + naam op bord, anders nabellen
- Ja:
- Hypo, maar wel aanspreekbaar
- BG < 4 mmol/L
- 15-20 gram koolhydraten
- BG < 4 mmol/L
- Gebruikt patient SU-derivaat/langwerkende insuline die hypo mogelijk veroorzaakt heeft?
- Patient 83 jaar, al jaren DM, temp 39.1, braken en diarree
- Braken = bellen! Cave HHS. DD Acuut MI (post aut propter)
- Visite + LO: gluc, pols, turgor? Inschatting of patient thuis kan blijven qua klinisch beeld en adequaat toezicht. Geen kwestie of het thuis zou kunnen. Vraag is: is thuisblijven in belang van de patiënt?
- Beleid: vochtintake belangrijker dan glucosewaarde! Indien duur klachten > 4 uur: echt insturen! Ook bij niet alert/adequaat genoeg.
- Eerste uur liefst 500ml, daarna 100-200ml vocht/uur
- 73 jaar, DM al jaren. VG: NSTEMI
- Empaglfozine 1dd25mg (SGLT2-remmer), Metformine 2dd1000mg, NPH insuline 1dd24E
- Fanatiek 5kg afgevallen, begrepen dat insuline daarmee verminderd kon worden, huisarts niet geinformeerd
- Temp 39.6, 2x gebraakt, gluc 8.9nn (eigenlijk normaal). Is suf/zichzelf niet. Dorst, geen eetlust, kortademig/benauwd, pijn in de rug, hoest niet
- Normoglycemische diabetische ketoacidose (DKA), door dehydratie en SGLT2-i-gebruik. Cave diepe acidose!
- insulinetekort + glycogeentekort icm glucosurie (70-80 gram glucose/dag)
- Dehydratie
- SADMAN: welke medicatie stoppen?
- SGLT-2-i, SU-derivaten (muv gliclazide ivm hepatische ipv renale uitscheiding) → acute nierschade/ketoacidose resp hypoglycemie
- diabetische normoglycemische ketoacidose → bij enige twijfel = insturen, belangrijk om precieze pH te weten gezien verder (opname)beleid
- ACE-remmer → acute nierschade
- Alle diuretica → acute nierschade
- Metformine → lactaatacidose
- ARBs → acute nierschade
- NSAIDs → acute nierschade
- Herstarten bij herstel normaal eten en drinken